Immunothérapie en oncologie ORL : un traitement qui s’appuie sur le système immunitaire pour détruire les cellules cancéreuses
L’immunothérapie anticancéreuse vise à activer et/ou stimuler le système immunitaire, afin qu’il s’attaque à la tumeur. Actuellement, un seul type de traitement est disponible en routine en cancérologie tête et cou, mais des études se penchent sur d’autres approches. Le point sur les immunothérapies contre les cancers ORL, avec le Dr Jérôme Fayette du Centre Léon Bérard, le Dr Joey Martin de l’Institut Curie et le Dr Yungan Tao de Gustave Roussy.
Introduite en oncologie depuis une vingtaine d’années, l’immunothérapie a déjà transformé la prise en charge de nombreux cancers. Les tumeurs de la tête et du cou en bénéficient, puisque des traitements existent déjà. De plus, la recherche avance à grands pas, dans le but de faire évoluer les pratiques et de soigner de plus en plus de patients.
Qu’est-ce que l’immunothérapie contre le cancer ?
« L’immunothérapie consiste à donner des armes au patient, afin que ce soit son système immunitaire qui fasse le travail et détruise la tumeur. Ce traitement ne fait rien directement aux cellules cancéreuses, contrairement à une chimiothérapie par exemple », explique le Dr Jérôme Fayette, oncologue médical au Centre Léon Bérard de Lyon.
Bien que les cellules tumorales soient anormales par rapport à des cellules saines, le système immunitaire ne les reconnaît pas toujours comme telles. Certaines cellules cancéreuses sont capables de déjouer les mécanismes de défense de l’organisme. Le principe de l’immunothérapie est donc de rétablir l’action du système immunitaire.
« L’immunothérapie consiste à donner des armes au patient, afin que ce soit son système immunitaire qui fasse le travail et détruise la tumeur. »
Quelles immunothérapies sont utilisées contre les cancers ORL ?
Une seule classe thérapeutique est utilisée actuellement en oncologie tête et cou : les inhibiteurs de checkpoints, ou inhibiteurs de points de contrôle, anti-PD1. Voici leur mode de fonctionnement : la cellule cancéreuse exprime un marqueur à sa surface, la protéine PDL1, qui s’accroche à un récepteur PD1 présent sur les cellules immunitaires. Une fois la liaison entre PDL1 et PD1 instaurée, le système immunitaire est paralysé. L’immunothérapie anti-PD1 lève ce blocage, pour restaurer un fonctionnement normal des défenses immunitaires.
Schéma mode d’action de l’immunothérapie anti-PD‑1
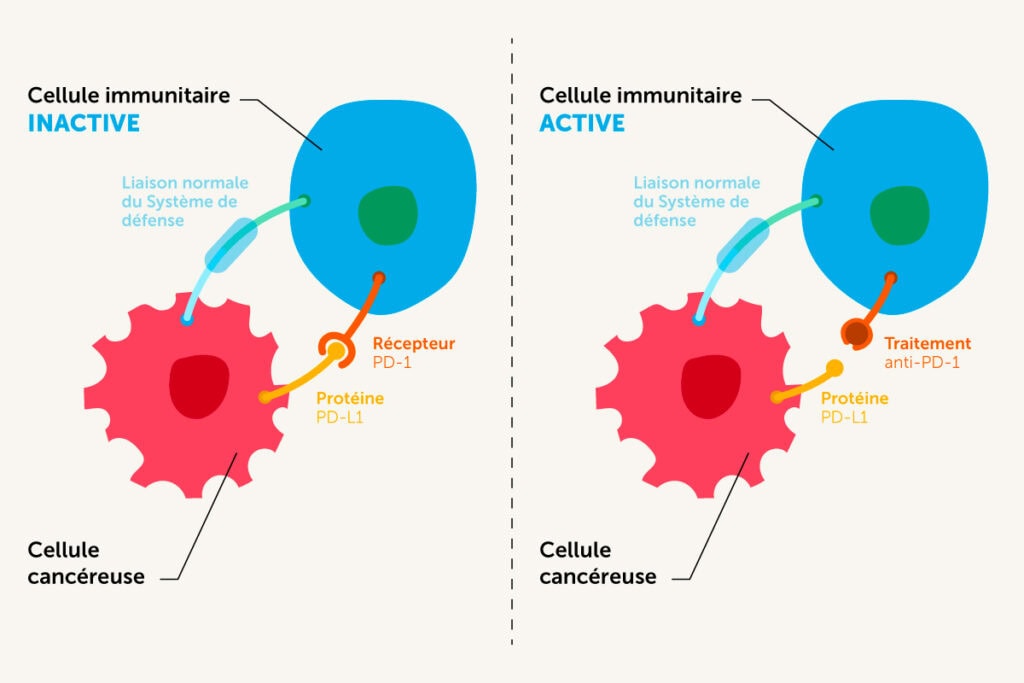
Environ 85 % des tumeurs ORL présentent la protéine PDL1 à leur surface. Un test est réalisé en amont des traitements d’immunothérapie, pour vérifier si le patient y est éligible ou non. De plus, il peut arriver que le marqueur PDL1 ne soit pas la seule voie de blocage du système immunitaire par le cancer. D’autres voies existent, mais elles ne sont pas connues pour l’instant. Cela explique que, parfois, les immunothérapies anti-PD1 ne sont pas efficaces, sans qu’il soit possible de le prévoir.
À ce jour, il existe deux médicaments anti-PD1 employés contre les cancers ORL en situation de récidive et/ou métastatique uniquement, administrés par voie intraveineuse : le pembrolizumab et le nivolumab.
Le pembrolizumab est indiqué pour des cancers PDL1 positifs (présentant le récepteur PDL1) n’ayant pas été traités par chimiothérapie au platine, ou en cas de récidive ou d’apparition de métastases plus de 6 mois après cette chimiothérapie. Le nivolumab est indiqué en cas d’échec de la chimiothérapie au platine, ou bien si une récidive ou des métastases sont observées moins de 6 mois après l’arrêt de la chimiothérapie.
En pratique, les oncologues peuvent réfléchir à adapter ces indications. Les décisions quant aux traitements les plus adaptés à chaque cas sont prises au cours d’une réunion de concertation pluridisciplinaire ou RCP.
Pour d’autres cancers, hors voies aérodigestives supérieures, l’immunothérapie par inhibiteurs de points de contrôle utilise des médicaments ciblant des marqueurs cellulaires différents. C’est le cas par exemple des anti-CTLA‑4 ou des anti-LAG‑3.
« Les anti-PD1 sont les seuls médicaments d’immunothérapie actuellement utilisés en oncologie ORL. »
» Découvrez notre dossier complet dédié à l’ensemble des traitements anticancer en ORL
Quels sont les effets secondaires des immunothérapies contre les cancers ORL ?
Ils sont les mêmes pour les cancers tête et cou que pour toute autre localisation. « Il peut arriver que le système immunitaire soit trop stimulé et s’attaque au patient lui-même au lieu de s’attaquer seulement à la tumeur », informe l’oncologue médical Dr Jérôme Fayette. Ces effets indésirables restent beaucoup plus rares que ceux d’autres traitements, comme les chimiothérapies. Les effets les plus graves, c’est-à-dire les toxicités de grade 3 et 4, touchent environ 15 % des personnes soignées par immunothérapie.
« Les effets indésirables des immunothérapie restent beaucoup plus rares que ceux d’autres traitements. »
Ces effets indésirables peuvent affecter tous les organes et toucher le système digestif, le système respiratoire, la peau, le foie, la thyroïde, les glandes surrénales, le pancréas, le cœur, etc. Les principaux effets secondaires s’observent à travers des toxicités digestives ou endocriniennes. Dans les cas les plus sévères, heureusement très rares, il est possible de voir se développer un diabète, des troubles cardiaques ou neurologiques.
En cas d’atteinte digestive ou respiratoire notamment, les symptômes sont généralement temporaires. « Un traitement immunosuppresseur peut être donné. Il est ensuite possible de décroître les doses et éventuellement de l’arrêter une fois que les symptômes ont disparu », continue le Dr Fayette.
L’oncologue du Centre Léon Bérard avise : « Les patients doivent être informés de ces effets indésirables, même s’ils sont rares, de manière à réagir très rapidement et à consulter. Par exemple, face à une diarrhée avec du sang, ou avec plus de 10 selles en 24 heures, il faut contacter immédiatement l’équipe médicale. »
Notez que les effets secondaires d’une immunothérapie surviennent parfois à distance, même plusieurs semaines après l’arrêt du traitement. Surveillance et vigilance s’imposent.
« Les patients doivent être informés de ces effets indésirables, même s’ils sont rares, de manière à réagir très rapidement et à consulter. »
Un autre type d’effet secondaire peut être observé lors de l’administration d’immunothérapies, durant ou juste après la perfusion : un « syndrome de relargage des cytokines » ou « syndrome de libération des cytokines ». Le système immunitaire, activé de manière trop importante, fabrique une grande quantité de molécules appelées « cytokines ». Ces dernières provoquent une inflammation accrue dans l’organisme et engendrent des complications légères à graves, allant de simples symptômes grippaux (fièvre, maux de tête, etc.) à des atteintes de différents organes. Les immunothérapies anti-PD1 ne sont pas vraiment concernées par ce relargage massif de cytokines, déclenché plutôt par d’autres types d’immunothérapies.
Immunothérapie et cancers ORL : où en est la recherche ?
Les anti-PD1 en péri-opératoire
Actuellement réservées en France aux cancers ORL récidivants ou métastatiques, les immunothérapies anti-PD1 pourraient bientôt concerner davantage de patients. Présentées lors du congrès de l’American Society Of Clinical Oncology (ASCO) en 2025, deux vastes études internationales de phase 3 viennent de démontrer l’intérêt de ces thérapies dans le cas de carcinomes épidermoïdes localement avancés résécables, donc des cancers primitifs et non des récidives. Les immunothérapies anti-PD1 augmentent de manière significative la survie sans événement. En d’autres termes, elles augmentent le pourcentage de patients qui ne présentent pas de récidive ni de métastase plusieurs années après l’arrêt du traitement.
« La première étude — KEYNOTE-689 — concerne l’injection de pembrolizumab en néo-adjuvant et en adjuvant, c’est-à-dire avant et après chirurgie, en complément du traitement standard par radiothérapie ou radio-chimiothérapie. La seconde — NIVOPOSTOP — concerne l’injection de nivolumab après chirurgie, en complément d’un traitement par radio-chimiothérapie », détaille le Dr Joey Martin, ORL à l’Institut Curie à Paris.
L’étude académique GORTEC 2018-01 NIVOPOSTOP a été menée dans six pays, dont la France, où elle a été coordonnée par le Dr Yungan Tao. L’onco-radiothérapeute de Gustave Roussy et président-élu du GORTEC (Groupe Oncologie Radiothérapie Tête Et Cou), commente : « Cette étude concerne des patients opérés d’un carcinome épidermoïde localement avancé de la bouche, de l’oropharynx, de l’hypopharynx ou du larynx, présentant au moins un facteur de haut risque de rechute. Deux groupes ont été constitués : le premier recevait le traitement standard par radio-chimiothérapie après chirurgie, le second recevait le nivolumab après chirurgie en plus du traitement standard par radio-chimiothérapie. » Conclusion : l’ajout du nivolumab a permis de diminuer de 24 % le risque de rechute et/ou de décès. Plus précisément, le taux de survie sans récidive ni métastase à 3 ans est passé de 52,3 % avec le traitement standard à 63,1 % avec l’ajout de l’immunothérapie.
« Dans l’étude GORTEC 2018-01 NIVOPOSTOP, les données de survie globale sont encore attendues. Cependant, l’ajout de l’immunothérapie aux traitements standards actuels pourrait très prochainement être amené à devenir le nouveau standard thérapeutique dans la prise en charge postopératoire des carcinomes épidermoïdes ORL localement avancés à haut risque de rechute », affirme le Dr Tao.
Suite à l’étude KEYNOTE-689, l’ajout du pembrolizumab avant et après chirurgie en complément du traitement standard pour ces patients est déjà approuvé aux États-Unis par la Food and Drug Administration (FDA) et au niveau européen, par l’Agence européenne des médicaments ou European Medicines Agency (EMA).
« L’ajout de l’immunothérapie aux traitements standards actuels pourrait très prochainement être amené à devenir le nouveau standard thérapeutique dans la prise en charge postopératoire des carcinomes épidermoïdes ORL localement avancés à haut risque de rechute. »
» Pour comprendre comment sont réalisés les essais cliniques, voici un article détaillé.
La recherche sur les anticorps bispécifiques
Il s’agit d’un autre type d’immunothérapie, dont le mode d’action est différent de celui des inhibiteurs de checkpoints. L’ORL Dr Joey Martin détaille : « À la différence des anti-corps monoclonaux, qui ciblent un seul marqueur à la surface des cellules tumorales et dont font partie les inhibiteurs de checkpoints, les anticorps bispécifiques s’accrochent à deux cibles distinctes. Ils peuvent inhiber le signal de prolifération tumorale, cibler les cellules tumorales responsables des récidives mais également déclencher une réaction immunitaire. »
Il n’existe pas encore d’anticorps bispécifiques employés en routine en oncologie ORL. Cependant, de nombreuses molécules sont en développement et trois d’entre elles semblent bien avancées. Elles présentent une cible commune : l’EGFR ou Epidermal Growth Factor Receptor, récepteur de facteur de croissance épidermique pouvant être retrouvé en quantité très importante à la surface des cellules cancéreuses. La seconde cible varie selon les médicaments développés, tous testés à ce jour sur des cancers ORL métastatiques ou en récurrence non-opérable.
Le petosemtamab, « l’un des plus prometteurs » selon le Dr Joey Martin, cible le récepteur LGR5. « La fixation à l’EGFR et au LGR5 à la surface de la cellule tumorale, permet une internalisation de l’anticorps et un meilleur blocage de l’action de l’EGFR, c’est-à-dire de la prolifération tumorale. Dans l’étude de phase 2, le médicament était associé à l’immunothérapie anti-PD1 pembrolizumab, et obtenait un taux de réponse de 60 %. » Le taux de réponse correspond au pourcentage de patients dont le cancer a régressé ou disparu après traitement.
Deux autres médicaments en phase d’essai suscitent l’intérêt : le ficerafusp alfa et l’amivantamab. Les résultats préliminaires sont très encourageants, mais des études à plus vaste échelle (en cours) devront les confirmer pour espérer des traitements accessibles aux patients.
» Pour approfondir le mécanisme d’action des anticorps et en savoir plus sur la recherche des anticorps-drogue conjugué, découvrez l’article à ce sujet
Un vaccin thérapeutique à l’étude en oncologie ORL
Son annonce avait fait grand bruit dans le courant de l’année 2025. Un vaccin thérapeutique (TG4050) a été testé en oncologie tête et cou chez des patients présentant un cancer résécable HPV-négatif. À la différence d’un vaccin préventif, un vaccin thérapeutique ne vise pas à empêcher l’apparition d’une maladie, mais à la soigner.
« Les vaccins thérapeutiques ne visent pas à empêcher l’apparition d’une maladie, mais à la soigner. Un vaccin thérapeutique contre les cancers ORL est à l’étude. »
Le Dr Joey Martin explicite : « Le vaccin thérapeutique en développement pour les cancers ORL est fabriqué à partir d’une biopsie de la tumeur, réalisée au moment de l’intervention chirurgicale de résection. Le laboratoire identifie 30 protéines exprimées par les cellules cancéreuses, les plus susceptibles de déclencher une réponse immunitaire, et développe un vaccin contenant ces protéines ou antigènes. Les injections du vaccin permettent de stimuler le système immunitaire afin qu’il reconnaisse et détruise de manière ciblée les cellules tumorales. »
Selon les premiers résultats, non seulement ce vaccin permettrait d’éviter les récidives, mais il offrirait aussi une protection durable après la dernière injection (caractérisée par la présence dans l’organisme de cellules immunitaires — des lymphocytes T — spécifiquement adaptées pour combattre la tumeur).
Une étude de phase 3 est en cours pour confirmer ces observations.
Les pistes de recherche sur les thérapies cellulaires
Le « transfert adoptif de cellules » consiste à apporter des cellules au patient afin qu’il bénéficie de leurs fonctions immunitaires. En cancérologie, deux thérapies sont en développement, déjà employées dans les cancers hématologiques : les cellules CAR‑T et les TILs.
Les cellules CAR‑T (pour Chimeric Antigenic Receptor — T) sont des cellules immunitaires appelées lymphocytes T, prélevées dans le sang du patient, génétiquement modifiées pour reconnaître et attaquer les cellules tumorales, puis réinjectées.
Les TILs (pour Tumor Infiltrating Lymphocytes ou lymphocytes d’infiltration tumorale) sont également des lymphocytes : de type B, T et NK pour « natural killers » ou « tueurs naturels ». Ces cellules immunitaires sont prélevées directement à l’intérieur de la tumeur cette fois. Elles présentent une spécificité : celle de reconnaître les cellules tumorales et de savoir comment les détruire. Le but ici est simplement de les multiplier en laboratoire, puis de les réinjecter.
Une étude de phase 2 publiée en août 2025, menée aux États-Unis auprès de patients souffrant d’un carcinome épidermoïde de la tête et du cou récidivant et/ou métastatique, a évalué l’intérêt d’une thérapie par TILs. « Le taux de contrôle de la maladie était de l’ordre de 76 % », selon le Dr Joey Martin, de l’Institut Curie.
Bien que forts intéressants, ces résultats restent très préliminaires et ne permettent pas d’envisager de traitement à court terme à base de TILs en oncologie tête et cou. Ils ouvrent tout de même la voie à de nouvelles recherches sur cette classe thérapeutique en plein développement.
Propos recueillis par Violaine Badie
POUR ALLER PLUS LOIN :
- Écouter le podcast sur les récidives avec le Docteur Burgy, oncologue ORL et Fabienne Kimmel, psycho-oncologue.
- Découvrir tous les soins de support permettant de soulager son quotidien.





