Cancers de l’oropharynx : diagnostic, traitements, surveillance
Les cancers oropharyngés liés au tabac et à l’alcool sont en baisse, quand ceux liés aux virus HPV augmentent. Ces derniers, de meilleur pronostic, pourraient prochainement se voir proposer des traitements moins lourds. Tout ce qu’il faut savoir sur ces cancers, avec les Prs Haitham Mirghani, ORL à l’Hôpital Européen Georges Pompidou à Paris, et Sébastien Thureau, onco-radiothérapeute au centre Henri Becquerel de Rouen.
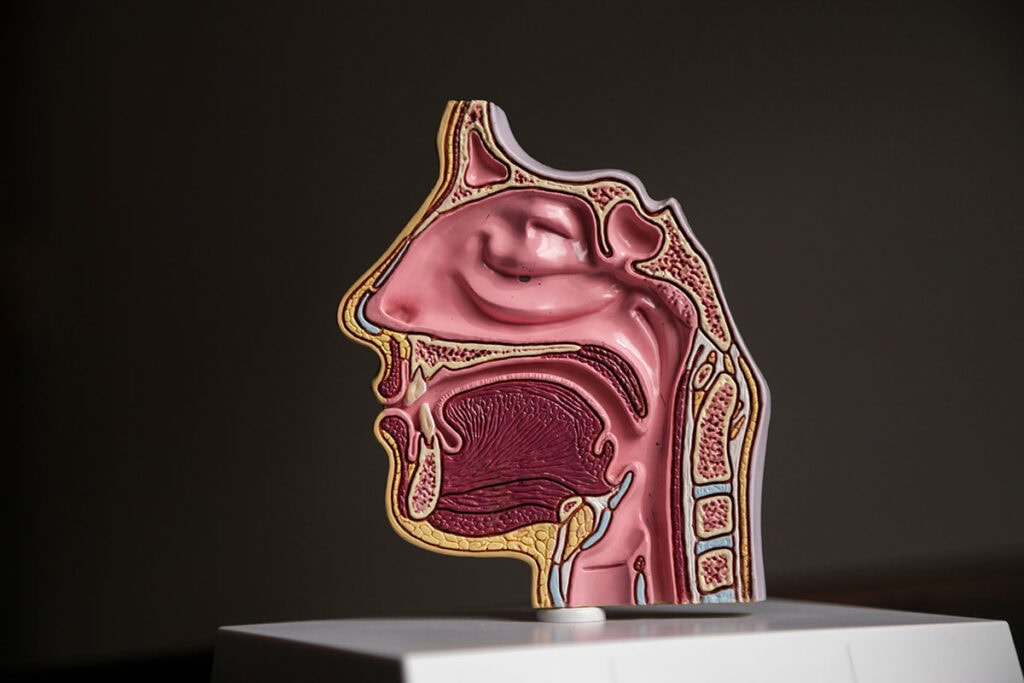
Qu’est-ce que l’oropharynx ?
« Schématiquement, le pharynx est un conduit, constitué à la fois de tissus qui tapissent l’intérieur de la paroi et de muscles, qui comprend plusieurs parties. La partie haute, derrière le nez est appelée rhinopharynx. La partie médiane, derrière la bouche, constitue l’oropharynx. La partie basse, derrière le larynx qui est l’organe contenant les cordes vocales, correspond à l’hypopharynx », décrit le Pr Haitham Mirghani, ORL spécialisé en chirurgie cervico-faciale.
Schéma des voies aérodigestives supérieures (VADS)
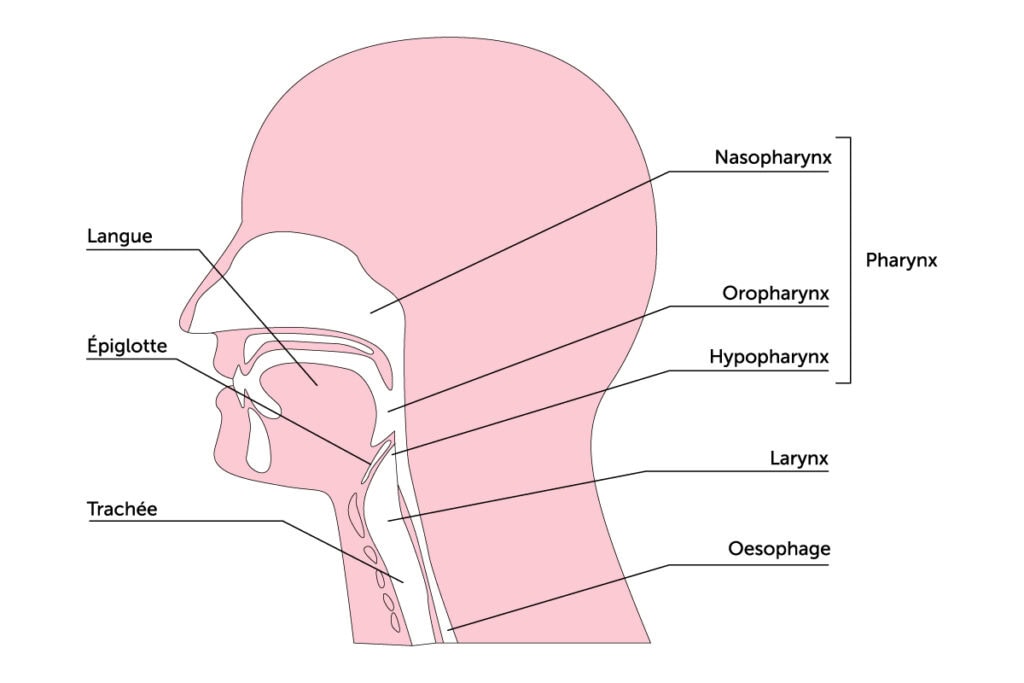
Cette zone oropharyngée comprend plusieurs structures anatomiques distinctes :
- le voile du palais en haut ;
- les amygdales palatines latéralement ;
- la base de la langue en bas, sur laquelle se trouve les amygdales linguales ;
- la paroi pharyngée en arrière.
L’oropharynx contribue à la fois à la parole, à la respiration et à la déglutition. La base de la langue est en effet primordiale pour propulser les aliments en arrière, pour protéger le larynx et éviter les fausses-routes vers les bronches.
Quels types de cancers peuvent toucher l’oropharynx ?
Le revêtement de l’orophraynx comprend plusieurs types de tissus. Le principal est l’épithélium (terme qui désigne les tissus de surface) dit “malpighien non kératinisé”. Cette appellation provient des regroupements cellulaires qui le composent (les corps de Malpighi). Il est “non kératinisé” car ne présente pas de kératine, à l’inverse de l’épiderme. On y retrouve aussi des structures appartenant au système lymphoïde (qui contient des cellules immunitaires, les amygdales, ainsi que des glandes salivaires accessoires).
Parmi les principaux cancers oropharyngés, on retrouve donc :
- des carcinomes épidermoïdes (90 à 95% des cas), qui se développent à partir de l’épithélium malpighien ou des cryptes amydaliennes (replis formés à leur surface) ;
- des lymphomes, qui touchent l’épithélium lymphoïde, ou des adénocarcinomes, qui touchent des glandes salivaires (beaucoup plus rares, 5 à 10 % des cas).
Quels sont les facteurs de risque ?
Au niveau de l’oropharynx, les cancers sont liés principalement :
- au tabac et à l’alcool pour les tumeurs qui se développent à partir de l’épithélium malpighien ;
- aux papillomavirus humains ou HPV, pour les tumeurs au niveau des amygdales. Il s’agit de la même famille de virus qui affecte la sphère génitale et est responsable des cancers du col de l’utérus, de la verge et de l’anus.
Il existe un grand nombre d’HPV différents, certains présentant un risque cancérigène, d’autres non. Les cancers liés au HPV dans l’oropharynx sont provoqués par la souche 16 dans près de 90% des cas.
« Le risque de décès est réduit de moitié pour un cancer oropharyngé HPV+ par rapport à un cancer de même stade HPV-. »
Cette distinction dans la cause des cancers oropharyngés revêt une importante majeure, comme l’atteste le Pr Mirghani : « Les altérations génétiques associées à l’apparition du cancer ne sont pas du tout les mêmes quand celui-ci est provoqué par le tabac ou par un papillomavirus. On considère que ce sont deux maladies totalement différentes. Les tumeurs liées au tabac sont plus agressives et peuvent être multiples car l’ensemble des voies aériennes et digestives a été affecté par les substances cancérigènes. De plus, les cancers liés au HPV, dits HPV positifs ou HPV+, induisent une réponse immunitaire bien plus importante que les cancers HPV négatifs ou HPV‑, ce qui est un facteur essentiel pour combattre les cellules cancéreuses. »
Ces différences expliquent en partie pourquoi les cancers oropharyngés HPV+ sont de bien meilleur pronostic. « Le risque de décès est réduit de moitié par rapport à un cancer de même stade HPV– .»
» Si vous souhaitez en savoir plus sur le papillomavirus, regardez la vidéo “Cancer ORL et HPV : un lien méconnu”
Le cancer de l’oropharynx en chiffres
En France, environ 5000 nouveaux cas de cancer oropharyngés sont diagnostiqués chaque année. Devenus les cancers de la gorge les plus fréquents, devant ceux du larynx, de l’hypopharynx et de la bouche, ils connaissent toutefois une légère baisse.
Cependant, cette diminution d’incidence nécessite une analyse un peu plus précise. « La part des cancers oropharyngés liés au tabac a tendance à se réduire, à l’instar des cancers du larynx et de l’hypopharynx, avec le recul du tabagisme. D’un autre côté, la part liée au HPV est en augmentation, ce qui compense beaucoup la baisse des cas liés au tabac », expose Haitham Mirghani.
Quelques explications possibles à cette hausse des cancers HPV+ : l’évolution des pratiques sexuelles (sexe oral), couplée à une très faible adhésion de la population française à la vaccination préventive anti-HPV. Selon l’Inserm*, « fin 2021, seules 45,8 % des jeunes filles de 15 ans et à peine 6 % des garçons du même âge avaient reçu au moins une dose du vaccin qui protège contre les infections par le papillomavirus humain ».
Pourtant les hommes constituent les principales victimes des cancers oropharyngés HPV+ (80 % des personnes touchées sont des hommes). « C’est aussi le cas pour les cancers provoqués par le tabac et l’alcool, puisque les hommes demeurent de plus gros consommateurs que les femmes », reconnaît le Pr Mirghani.
La moyenne d’âge de survenue de ces cancers est de 50–60 ans. Toutefois, ils peuvent s’observer chez des patients plus jeunes ou plus âgés.
Symptômes et diagnostic
Là encore, les symptômes sont susceptibles de différer selon la cause de la tumeur. L’ORL Haitham Mirghani éclaire : « Pour les personnes qui fument et boivent, le premier symptôme est souvent une douleur dans la gorge, parfois spontanée, parfois à la déglutition, associée ou non au développement d’une boule dans le cou. » Un tableau que l’expert décrit comme « très parlant cliniquement ».
Un cancer oropharyngé engendré par la présence persistante d’un papillomavirus provoque des symptômes plus subjectifs, avec : « Peu, voire pas, de douleur ou une simple gêne dans la gorge. Pour beaucoup de patients, l’apparition d’une boule dans le cou est le symptôme principal. Ce tableau affectant souvent des personnes n’ayant jamais fumé (près de 50% des cas), les médecins ne pensent pas toujours à un cancer, ce qui peut retarder le diagnostic », regrette le Pr Mirghani.
Son message à faire passer est clair : en cas de douleur, de gêne, d’apparition d’une boule dans le cou, qui persistent au-delà de 3 semaines, il ne faut pas hésiter à consulter !
» Découvrez les symptômes sur la tête et du cou, et la règle du 1 pour 3, dans cet article à ce sujet
« Le diagnostic est dans un premier temps clinique et visuel, en regardant le fond de la gorge avec un abaisse-langue ou à l’aide d’un fibroscope. Les lésions cancéreuses peuvent présenter un aspect ulcéré, bourgeonnant, ou les deux. » Le diagnostic de cancer nécessite ensuite une biopsie. Un bilan d’extension complet est également réalisé pour déterminer précisément les limites de la lésion tumorale et les éventuelles tumeurs à distance. Il est désormais préconisé de réaliser un test complémentaire, afin de savoir si le cancer est causé ou non par un papillomavirus.
Les traitements possibles d’un cancer oropharyngé
Les médecins disposent de plusieurs armes thérapeutiques face à un cancer de l’oropharynx. Beaucoup de facteurs entrent en jeu dans leur prise de décision : l’âge du patient, son état général, ses comorbidités, la localisation de la tumeur, l’infiltration dans les tissus avoisinants, si les ganglions du cou sont atteints ou non… Le choix de la meilleure option thérapeutique se fait toujours au cas par cas, au sein d’une réunion de concertation pluridisciplinaire à laquelle participent plusieurs spécialistes (chirurgien ORL, onco-radiothérapeute, oncologue médical, radiologue, anatomopathologiste, etc.).
Parmi les traitements possibles, peuvent être proposées :
- des monothérapies, souvent pour les petites tumeurs : soit chirurgie seule, soit radiothérapie seule ;
- des polythérapies : combinaison de chirurgie + radiothérapie, combinaison de radiothérapie + chimiothérapie ou combinaison de chirurgie + radio-chimiothérapie.
En cas de tumeur non-guérissable (trop grosse, trop avancée ou métastatique), une association d’immunothérapie et de chimiothérapie est souvent prescrite.
« Pour des tumeurs localisées ou localement avancées, nous pouvons adopter une stratégie différente selon le statut HPV+ ou HPV-. En effet, les cancers HPV+ sont plus sensibles à la radio-chimiothérapie qui peut alors être privilégiée pour limiter les toxicités des traitements », informe le Pr Sébastien Thureau, onco-radiothérapeute. L’avantage ? « Éviter la chirurgie et ses conséquences parfois lourdes. » Là encore, le choix de cette option de traitement reste toujours conditionné à de nombreux facteurs.
À l’heure actuelle, il s’agit de la seule distinction thérapeutique entre les cancers HPV+ et HPV-. Des essais en cours pourraient amener à recommander des protocoles de traitements différents. Selon le Pr Thureau : « Nous sommes dans une démarche d’optimisation et de réduction de la thérapeutique. Par exemple, un essai clinique actuel cherche à déterminer si les cancers liés au HPV pourraient être traités avec une chirurgie et des doses de radiothérapie adjuvante plus faibles ou sans chimiothérapie. Nous espérons dans quelques mois voire quelques années aller vers une désescalade thérapeutique. »
Un vaccin thérapeutique anti-HPV 16 est également en cours de développement. Contrairement aux vaccins préventifs, dont l’objectif est d’éviter la contamination, les vaccins thérapeutiques visent à éliminer le virus présent dans les cellules.
« Nous espérons dans quelques mois voire quelques années aller vers une désescalade thérapeutique. »
Effets secondaires et qualité de vie après traitement
« Dans le cas d’un cancer de l’oropharynx, la chirurgie peut entraîner des troubles de la déglutition ou de la parole et avoir un impact physique assez lourd », précise le Pr Sébastien Thureau. Les techniques chirurgicales de moins en moins invasives et les méthodes de reconstruction de plus en plus avancées contribuent à réduire ces risques.
Parmi les effets aigus d’une radiothérapie, le spécialiste Sébastien Thureau cite les mucites, inflammations de la muqueuse de la gorge qui surviennent généralement après 3 à 4 semaines de traitement. « Nous n’avons pas, pour l’heure, le moyen d’éviter ces mucites, mais nous pouvons les prendre en charge en proposant des séances de photobiomodulation concomitantes aux rayons afin de réduire les douleurs. » Des progrès considérables ont déjà été réalisés depuis quelques années pour atténuer les effets secondaires des rayons (optimisation des doses, meilleur ciblage).
Les mucites peuvent mener à envisager une alimentation par sonde naso-gastrique ou par gastrostomie afin de pallier les difficultés à s’alimenter. « Le retour à la normale peut être un peu long, parfois plusieurs semaines à plusieurs mois après l’arrêt de la radiothérapie », admet l’onco-radiothérapeute. L’alimentation est un critère déterminant d’un bon rétablissement. « Il est nécessaire d’éviter au maximum la perte de poids pendant les traitements, car elle est souvent associée à une perte musculaire. »
Deux effets secondaires fréquents sont aussi à noter sur le long terme : l’hyposialie (baisse de la quantité et de la qualité de la salive) voire l’asialie (absence de salive), et les troubles dentaires. Ces derniers sont intimement liés au manque de salive, qui joue un rôle protecteur de l’émail. Là encore, des solutions existent. Des gouttières fluorées peuvent être proposées aux personnes présentant des fragilités dentaires.
Parmi les effets secondaires au long court, d’autres peuvent s’avérer plus sévères comme des troubles persistants de la déglutition (8 à 10 % des cas) ou encore une nécrose de l’os de la mâchoire (5% des cas).
La qualité de vie après traitements dépend en grande partie de l’importance de la tumeur oropharyngée initiale et de son extension. Plus elle est diagnostiquée tôt, donc de petite taille, plus les séquelles seront minimisées. Se tourner vers les soins de support fait aussi partie des recommandations, à la fois pour mieux vivre les traitements et pour réduire autant que possible leurs effets secondaires immédiats et tardifs. Le Pr Thureau mentionne des exemples qui invitent à l’optimisme : « J’ai soigné des patients pour des cancer oropharyngés HPV+ par exemple, avec des traitements uniquement de radio-chimiothérapie, dont il est impossible de dire qu’ils ont été malades. »
» S’informer davantage sur les cancers ORL / VADS en visionnant ce webinar proposé par le centre Henri Becquerel.
Quel suivi après un cancer oropharyngé ?
« Entre 3 et 4 mois après la fin des traitements, un scanner et une IRM sont prescrits. Ensuite, si la maladie a disparu, le suivi se fera principalement via un examen clinique », renseigne l’ORL Haitham Mirghani. La fréquence de suivi recommandée par la Société Française d’Oto-Rhino-Laryngologie et de Chirurgie de la Face et du Cou est la suivante :
- un examen systématique tous les 2 mois la 1ère année ;
- puis tous les 3 mois la 2e année ;
- puis tous les 4 mois la 3e année ;
- puis tous les 6 mois la 4e et la 5e années ;
- puis tous les ans.
Un scanner pulmonaire est également préconisé chaque année pour les fumeurs et anciens fumeurs.
Le risque de récidive demeure faible pour les cancers HPV+ : « 80 à 90 % des patients vont guérir et ne pas rechuter », indique le Pr Mirghani. Pour les cancers liés au tabac, le risque de récidive (au niveau de la gorge ou en termes de métastases) est de l’ordre de 50 %.
« Pour les cancers HPV+, 80 à 90 % des patients vont guérir et ne pas rechuter. »
Comme pour chaque type de cancer, l’intérêt majeur réside dans la détection la plus précoce possible de ces récidives. « Dans les cancers du sein, de la prostate ou encore de la thyroïde, des marqueurs sanguins aident à la surveillance. Dès que ces protéines augmentent, elles sont le signe d’une éventuelle récidive et il est possible de réagir très vite. Nous testons actuellement un biomarqueur qui nous offrirait la même opportunité avec les cancers de la gorge en lien avec un papillomavirus », développe le médecin ORL. Ce biomarqueur : l’ADN d’HPV circulant.
« Quand une personne est simplement infectée par un papillomavirus, ce qui est très fréquent, son ADN ne se retrouve pas dans le sang. En revanche, en cas de cancer lié aux HPV, les cellules tumorales érodent les vaisseaux et relarguent leur contenu, donc de l’ADN d’HPV se retrouve dans la circulation sanguine. Un patient soigné ne présente plus d’ADN d’HPV dans son sang. Si on retrouve cet ADN sur une prise de sang, c’est le signe que la maladie est en train de repartir. »
Inclure cette surveillance par dosage sanguin pourrait être une piste d’amélioration du suivi des cancers HPV+. À l’automne 2023, le Pr Mirghani coordonnera avec le Pr Blanchard une étude française randomisée (baptisée « SURVEILLE HPV ») destinée à tester un nouveau protocole de suivi. « Nous comparerons la surveillance standard à une surveillance avec deux fois moins de rendez-vous, mais avec dosage sanguin de l’ADN d’HPV circulant à chaque consultation. Si le résultat est positif, nous réaliserons des examens d’imagerie supplémentaires : scanner du cou et thorax et TEP-scanner. » Au-delà de l’intérêt manifeste pour détecter précocement les récidives, ce protocole de suivi, s’il s’avère efficace, permettrait de réduire le nombre de rendez-vous, parfois contraignants pour les patients.
Propos recueillis par Violaine Badie
POUR ALLER PLUS LOIN :
- Lire les dernières recommandations de la Haute Autorité de Santé sur la vaccination contre le papillomavirus (MAJ 2025).
- Découvrir Demain Sans HPV, un collectif de 10 associations pour soutenir la prévention des cancers liés aux papillomavirus.
- Écouter le témoignage de Denis, touché par un cancer de l’oropharynx en 2021.





